Diferència entre les revisions de "Àtom"
Text reemplaça - 'Referencies' a 'Referències' |
Sense resum d'edició |
||
| (No es mostren 3 edicions intermiges d'3 usuaris) | |||
| Llínea 72: | Llínea 72: | ||
Fon el primer model atòmic en bases científiques, fon formulat en l'any [[1808]] per [[John Dalton]], qui imaginava als àtoms com a diminutes esferes.<ref>Racó Arce, Alvaro (1983) ABC de Química Primer Curs, Editorial Herrero, Mèxic, ISBN: 968-420-294-6.</ref> Este primer model atòmic postulava: | Fon el primer model atòmic en bases científiques, fon formulat en l'any [[1808]] per [[John Dalton]], qui imaginava als àtoms com a diminutes esferes.<ref>Racó Arce, Alvaro (1983) ABC de Química Primer Curs, Editorial Herrero, Mèxic, ISBN: 968-420-294-6.</ref> Este primer model atòmic postulava: | ||
* La matèria està formada per partícules molt chicotetes | * La matèria està formada per partícules molt chicotetes nomenades àtoms, que són indivisibles i no es poden destruir. | ||
* Els àtoms d'un mateix element són iguals entre si, tenen el seu propi pes i calitats pròpies. Els àtoms dels diversos elements tenen pesos diferents. | * Els àtoms d'un mateix element són iguals entre si, tenen el seu propi pes i calitats pròpies. Els àtoms dels diversos elements tenen pesos diferents. | ||
* Els àtoms permaneixen sense divisió, encara que es combinen en les reaccions químiques. | * Els àtoms permaneixen sense divisió, encara que es combinen en les reaccions químiques. | ||
| Llínea 133: | Llínea 133: | ||
En el model de Schrödinger s'abandona la concepció dels electrons com a esferes diminutes en càrrega que giren entorn del núcleu, que és una extrapolació de l'experiència a nivell macroscòpic cap a les diminutes dimensions de l'àtom. En conte d'açò, Schrödinger descriu als electrons per mig d'una [[funció d'ona]], el quadrat de la qual representa la ''provabilitat de presència'' en una regió delimitada de l'espai. Esta zona de provabilitat es coneix com [[orbital atòmic|orbital]]. La gràfica següent mostra els orbitals per als primers nivells d'energia disponibles en l'àtom d'hidrogen. | En el model de Schrödinger s'abandona la concepció dels electrons com a esferes diminutes en càrrega que giren entorn del núcleu, que és una extrapolació de l'experiència a nivell macroscòpic cap a les diminutes dimensions de l'àtom. En conte d'açò, Schrödinger descriu als electrons per mig d'una [[funció d'ona]], el quadrat de la qual representa la ''provabilitat de presència'' en una regió delimitada de l'espai. Esta zona de provabilitat es coneix com [[orbital atòmic|orbital]]. La gràfica següent mostra els orbitals per als primers nivells d'energia disponibles en l'àtom d'hidrogen. | ||
<br clear="all" /> | <br clear="all" /> | ||
== Referències == | == Referències == | ||
{{listaref}} | {{listaref}} | ||
| Llínea 147: | Llínea 147: | ||
}}. | }}. | ||
* [http://public.web.cern.ch/public/Content/Chapters/AboutCERN/WhyStudyPrtcles/UniverseBricks/UniverseBricks-en.Html Bricks of the Universe: the Building Blocks of Matter] (material divulgatiu del [[CERN]]). | * [http://public.web.cern.ch/public/Content/Chapters/AboutCERN/WhyStudyPrtcles/UniverseBricks/UniverseBricks-en.Html Bricks of the Universe: the Building Blocks of Matter] (material divulgatiu del [[CERN]]). | ||
== Vore també == | == Vore també == | ||
| Llínea 159: | Llínea 159: | ||
== Enllaços externs == | == Enllaços externs == | ||
*[http://www.energia.4d2.net/ Energia nuclear: el poder de l'àtom] | * [http://www.energia.4d2.net/ Energia nuclear: el poder de l'àtom] | ||
== Referències== | == Referències== | ||
Última revisió del 09:37 17 dec 2024

En química i física, àtom (del llatí atomum, i este del grec ἄτομον, indivisible)[1] és la unitat més chicoteta d'un element químic que manté la seua identitat o les seues propietats i que no és possible dividir per mig de processos químics.
El concepte d'àtom com a bloc bàsic i indivisible que compon la matèria de l'univers ya fon postulat per la escola atomista en l'Antiga Grècia. No obstant, la seua existència no va quedar demostrada fins al sigle XIX. En el desenroll de la física nuclear en el sigle XX es va comprovar que l'àtom pot subdividir-se en partícules més chicotetes.[2][3]
Estructura atòmica
[editar | editar còdic]La teoria acceptada hui és que l'àtom es compon d'un núcleu de carrega positiva format per protons i neutrons, en conjunt coneguts com nucleó, al voltant del qual es troba un núvol d'electrons de càrrega negativa.
El núcleu atòmic
[editar | editar còdic]El núcleu de l'àtom es troba format per nucleons, els quals poden ser de dos classes:
- Protons: Partícula de càrrega elèctrica positiva igual a una càrrega elemental, i 1,67262 × 10–27 kg i una massa 1837 vegades major que la de l'electró.
- Neutrons: Partícules carents de càrrega elèctrica i una massa un poc major que la del protó (1,67493 × 10–27 kg).
El núcleu més senzill és el de l'hidrogen, format únicament per un protó. El núcleu del següent element en la taula periòdica, l'heli, es troba format per dos protons i dos neutrons. La cantitat de protons contingudes en el núcleu de l'àtom es coneix com número atòmic, el qual es representa per la lletra Z i s'escriu en la part inferior esquerra del símbol químic. És el que distinguix a un element químic d'un atre. Segons lo descrit anteriorment, el número atòmic de l'hidrogen és 1 (1H), i el de l'heli, 2 (2He).
La cantitat total de nucleons que conté un àtom es coneix com número màssic, representat per la lletra a i escrit en la part superior esquerra del símbol químic. Per als eixemples donats anteriorment, el número màssic de l'hidrogen és 1(1H), i el de l'heli, 4(4He).
Existixen també àtoms que tenen el mateix número atòmic, pero diferent número màssic, els quals es coneixen com isòtops. Per eixemple, hi ha tres isòtops naturals de l'hidrogen, el proti (1H), el deuteri (2H) i el triti (3H). Tots posseïxen les mateixes propietats químiques de l'hidrogen, i poden ser diferenciats únicament per certes propietats físiques.
Atres térmens menys utilisats relacionats en l'estructura nuclear són els isótons, que són àtoms en el mateix número de neutrons. Els isóbars són àtoms que tenen el mateix número màssic.
Pel fet de que els protons tenen càrregues positives s'haurien de repelir entre si, no obstant, el núcleu de l'àtom manté la seua cohesió degut a l'existència d'una atra força de major magnitut, encara que de menor abast coneguda com l'interacció nuclear forta.
Interaccions elèctriques entre protons i electrons
[editar | editar còdic]Abans de l'experiment de Rutherford la comunitat científica acceptava el model atòmic de Thomson, situació que varià despuix de l'experiència de Rutherford. Els models posteriors es basen en una estructura dels àtoms en una massa central carregada positivament rodejada d'un núvol de càrrega negativa.[4]
Este tipo d'estructura de l'àtom va portar a Rutherford a propondre el seu model en que els electrons es mourien al voltant del núcleu en òrbites. Este model té una dificultat provinent del fet que una partícula carregada accelerada, com seria necessari per a mantindre's en òrbita, radiaria radiació electromagnètica, perdent energia. Les lleis de Newton, junt en l'equació de Maxwell de l'electromagnetisme aplicades a l'àtom de Rutherford porten que en un temps de l'orde de 10-10 s, tota l'energia de l'àtom s'hauria radiat, en la consegüent caiguda dels electrons sobre el núcleu.[5]
Núvol electrònic
[editar | editar còdic]Entorn al núcleu es troben els electrons que són partícules elementals de càrrega negativa igual a una càrrega elemental i en una massa de 9,10 × 10–31 kg
La cantitat d'electrons d'un àtom en el seu estat basal és igual a la cantitat de protons que conté en el núcleu, és dir, al número atòmic, per lo qual un àtom en estes condicions té una càrrega elèctrica neta igual a 0.
A diferència dels nucleons, un àtom pot perdre o adquirir alguns dels seus electrons sense modificar la seua identitat química, transformant-se en un ió, una partícula en càrrega neta diferent de zero.
El concepte de que els electrons es troben en òrbites satelitals al voltant del núcleu s'ha abandonat en favor de la concepció d'un núvol d'electrons deslocalisats o difusos en l'espai, el qual representa millor el comportament dels electrons descrit per la mecànica quàntica únicament com a funcions de densitat de provabilitat de trobar un electró en una regió finita d'espai al voltant del núcleu.
Dimensions atòmiques
[editar | editar còdic]La major part de la massa d'un àtom es concentra en el núcleu, format pels protons i els neutrons, abdós coneguts com nucleons, els quals són 1836 i 1838 vegades més pesats que l'electró respectivament.
El tamany o volum exacte d'un àtom és difícil de calcular, ya que els núvols d'electrons no conten en bordells definits, pero pot estimar-se raonablement en 1,0586 × 10–10 m, el doble del ràdio de Bohr per a l'àtom d'hidrogen. Si açò es compara en el tamany d'un protó, que és l'única partícula que compon el núcleu de l'hidrogen, que és aproximadament 1 × 10–15 es veu que el núcleu d'un àtom és prop de 100.000 vegades menor que l'àtom mateix, i no obstant, concentra pràcticament el 100% de la seua massa.
Per a efectes de comparació, si un àtom tinguera el tamany d'un estadi, el núcleu seria del tamany d'una boleta colocada en el centre, i els electrons, com a partícules de pols agitada pel vent al voltant dels assents.
Història de la teoria atòmica
[editar | editar còdic]El concepte d'àtom existix des de l'Antiga Grècia propost pels filòsofs grecs Demòcrit, Leucip i Epicur, no obstant, no es va generar el concepte per mig de l'experimentació sino com una necessitat filosòfica que explicara la realitat, ya que, com proponien estos pensadors, la matèria no podia dividir-se indefinidament, per lo qual havia d'existir una unitat o bloc indivisible i indestructible que al combinar-se de diferents formes creara tots els cossos macroscòpics que nos rodegen.[6] El següent alvanç significatiu no es realisà fins que en l'any 1773 el químic francés Antoine-Laurent de Lavoisier va postular el seu enunciat: "La matèria no es crea ni es destruïx, simplement es transforma."; demostrat més tart pels experiments del químic anglés John Dalton qui en l'any 1804, despuix de medir la massa dels reactius i productes d'una reacció, i va concloure que les substàncies estan compostes d'àtoms esfèrics idèntics per a cada element, pero diferents d'un element a un atre.[7]
Despuix en l'any 1811 Amedeo Avogadro, físic italià, va postular que a una temperatura, pressió i volum donats, un gas conté sempre el mateix número de partícules, siguen àtoms o molècules, independentment de la naturalea del gas, fent al mateix temps l'hipòtesis de que els gasos són molècules poliatòmiques en lo que es va començar a distinguir entre àtoms i molècules.[8]
El químic rus Dmítri Ivánovich Mendeléyev creà en 1869 una classificació dels elements químics en orde creixent de la seua massa atòmica, remarcant que existia una periodicitat en les propietats químiques. Este treball fon el precursor de la taula periòdica dels elements com la coneixem actualment.[9]
La visió moderna de la seua estructura interna va haver d'esperar fins a l'experiment de Rutherford en 1911 i el model atòmic de Bohr. Posteriors descobriments científics, com la teoria quàntica, i avanços tecnològics, com el microscopi electrònic, han permés conéixer en major detall les propietats físiques i químiques dels àtoms.[10]
Evolució del model atòmic
[editar | editar còdic]

La concepció de l'àtom que s'ha tengut a lo llarc de l'història ha variat d'acort en els descobriments realisats en el camp de la física i la química. A continuació es farà una exposició dels models atòmics proposts pels científics de diferents époques. Alguns d'ells són completament obsolets per a explicar els fenòmens observats actualment, pero s'inclouen a manera de resenya històrica.
Model de Dalton
[editar | editar còdic]Fon el primer model atòmic en bases científiques, fon formulat en l'any 1808 per John Dalton, qui imaginava als àtoms com a diminutes esferes.[11] Este primer model atòmic postulava:
- La matèria està formada per partícules molt chicotetes nomenades àtoms, que són indivisibles i no es poden destruir.
- Els àtoms d'un mateix element són iguals entre si, tenen el seu propi pes i calitats pròpies. Els àtoms dels diversos elements tenen pesos diferents.
- Els àtoms permaneixen sense divisió, encara que es combinen en les reaccions químiques.
- Els àtoms, al combinar-se per a formar composts guarden relacions simples.
- Els àtoms d'elements diferents es poden combinar en proporcions distintes i formar més d'un compost.
- Els composts químics es formen a l'unir-se àtoms de dos o més elements distints.
No obstant va desaparéixer davant del model de Thomson ya que no explica els rajos catòdics, la radioactivitat ni la presència dels electrons (e-) o protons(p+).
Model de Thomson
[editar | editar còdic]
Despuix del descobriment de l'electró en l'any 1897 per Joseph John Thomson, es determinà que la matèria es componia de dos parts, una negativa i una positiva. La part negativa estava constituïda per electrons, els quals es trobaven segons este model immersos en una massa de càrrega positiva a manera de panses en un pastiç (de l'analogia de l'anglés plum-pudding model) o raïm en gelatina. Posteriorment Jean Perrin va propondre un model modificat a partir del de Thompson a on les "panses" (electrons) se situaven en la part exterior del "pastiç" (la càrrega positiva).
Detalls del model atòmic
[editar | editar còdic]Per a explicar la formació d'ions, positius i negatius, i la presència dels electrons dins de l'estructura atòmica, Thomson va idear un àtom semblant a un pastiç de fruites. Un núvol positiu que contenia les chicotetes partícules negatives (els electrons) suspesos en ella. El número de càrregues negatives era l'adequat per a neutralisar la càrrega positiva. En el cas que l'àtom perdera un electró, l'estructura quedaria positiva; i si guanyava, la càrrega final seria negativa. D'esta manera, explicava la formació d'ions; pero deixà sense explicació l'existència de les atres radiacions.
Model de Rutherford
[editar | editar còdic]- Artícul principal → Modelo atòmic de Rutherford.
Este model fon desenrollat pel físic Ernest Rutherford a partir dels resultats obtenguts en el que hui es coneix com el experiment de Rutherford en 1911. Representa un alvanç sobre el model de Thomson, ya que manté que l'àtom es compon d'una part positiva i una negativa, no obstant, a diferència de l'anterior, postula que la part positiva es concentra en un núcleu, el qual també conté virtualment tota la massa de l'àtom, mentres que els electrons s'ubiquen en una corfa orbitant al núcleu en òrbites circulars o elíptiques en un espai buit entre ells. A pesar de ser un model obsolet, és la percepció més comú de l'àtom del públic no científic.
Rutherford va predir l'existència del neutró l'any 1920, per eixa raó en el model anterior (Thomson), no es parla d'este.
Per desgràcia, el model atòmic de Rutherford presentava diverses incongruències:
- Contradia les lleis de l'electromagnetisme de James Clerk Maxwell, les quals estaven molt comprovades per mig de senyes experimentals. Segons les lleis de Maxwell, una càrrega elèctrica en moviment (en este cas l'electró) hauria d'emetre energia constantment en forma de radiació i arribaria un moment en que l'electró cauria sobre el núcleu i la matèria es destruiria. Tot ocorreria molt breument.
- No explicava els espectres atòmics.
Model de Bohr
[editar | editar còdic]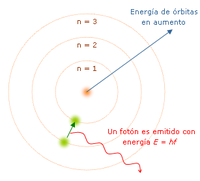
Este model és estrictament un model de l'àtom d'hidrogen prenent com a punt de partida el model de Rutherford, Niels Bohr tracta d'incorporar els fenòmens d'absorció i emissió dels gasos, aixina com la nova teoria de la quantisació de l'energia desenrollada per Max Planck i el fenomen de l'efecte fotoelèctric observat per Albert Einstein.
“L'àtom és un chicotet sistema solar en un núcleu en el centre i electrons movent-se al voltant del núcleu en òrbites ben definides.” Les òrbites estan quantisades (els e- poden estar a soles en certes òrbites)
- Cada orbita té una energia associada. La més externa és la de major energia.
- Els electrons no radien energia (llum) mentres permaneixen en òrbites estables.
- Els electrons poden botar d'una a una atra orbita. Si ho fan des d'una de menor energia a una de major energia absorbix un quant d'energia (una cantitat) igual a la diferència d'energia associada a cada orbita. Si passa d'una de major a una de menor, pert energia en forma de radiació (llum).
El major èxit de Bohr fon donar l'explicació a l'espectre d'emissió de l'hidrogen. Pero a soles la llum d'este element. Proporciona una base per al caràcter quàntic de la llum, el fotó és emés quan un electró cau d'una orbita a una atra, sent un pols d'energia radiada. Bohr no pot explicar l'existència d'òrbites estables i per a la condició de quantisació. Bohr trobà que el moment angular de l'electró és h/2p per un método que no pot justificar.
Model de Schrödinger: model actual
[editar | editar còdic]
Despuix que Louis-Victor de Broglie va propondre la naturalea ondulatòria de la matèria en l'any 1924, la qual fon generalisada per Erwin Schrödinger en 1926, es va actualisar novament el model de l'àtom.
En el model de Schrödinger s'abandona la concepció dels electrons com a esferes diminutes en càrrega que giren entorn del núcleu, que és una extrapolació de l'experiència a nivell macroscòpic cap a les diminutes dimensions de l'àtom. En conte d'açò, Schrödinger descriu als electrons per mig d'una funció d'ona, el quadrat de la qual representa la provabilitat de presència en una regió delimitada de l'espai. Esta zona de provabilitat es coneix com orbital. La gràfica següent mostra els orbitals per als primers nivells d'energia disponibles en l'àtom d'hidrogen.
Referències
[editar | editar còdic]- ↑ «Àtom», en Diccionari de la Llengua Espanyola (22a ed.). Real Acadèmia Espanyola (2001). Consultat el 20 de juliol del 2009.
- ↑ Haubold, Hans; Mathai, A. M. (1998). «Microcosmos: From Leucippus to Yukawa». Structure of the Universe. Common Sense Science. Consultat el 2008-01-17.
- ↑ Harrison (2003:123–139).
- ↑ Antonio Rañada(1990), Dinàmica Clàssica. Madrid, Aliança Editorial, S. A. 84-206-8133-4
- ↑ B.H. Bransden and C.J. Joachain (1992), Physics of Àtoms and Molecules. Harlow-Essex-England, Longman Group Limited. 0-582-44401-2
- ↑ presocraticos/Atomistes/lligueels meus.Html Filòsofs Presocràtics: Atomistes, Leucipo i Demòcrit
- ↑ Protagonistes de la revolució:Lavoisier, A.L.
- ↑ Amedeo Avogadro (en italià)
- ↑ Elements and Atoms: Chapter 12: Mendeleev's First Periodic Table (en anglés)
- ↑ Experiment de Rutherford
- ↑ Racó Arce, Alvaro (1983) ABC de Química Primer Curs, Editorial Herrero, Mèxic, ISBN: 968-420-294-6.
- Cronologia del model atòmic (en anglés).
- Sokolovsky, Silvia (2002). «L'Àtom»..
- Bricks of the Universe: the Building Blocks of Matter (material divulgatiu del CERN).
Vore també
[editar | editar còdic]- Molècula
- Taula periòdica dels elements
- Model estàndart de física de partícules
- Fissió i fusió nuclear
- Accelerador de partícules
- Medicina nuclear
- Arma nuclear
Enllaços externs
[editar | editar còdic]Referències
[editar | editar còdic]- Est artícul fon creat a partir de la traducció de l'artícul es.wikipedia.org/wiki/Átomo de la Wikipedia en espanyol, baix llicència Creative Commons-BY-SA.

